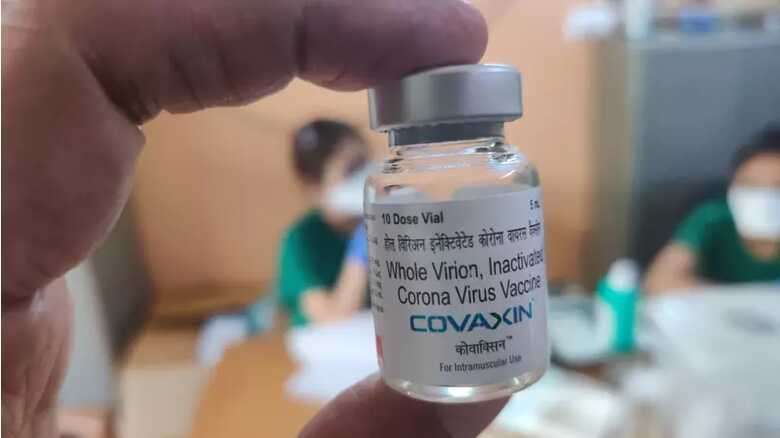
A Agência Nacional de Vigilância Sanitária (Anvisa) recebeu nesta terça-feira (29) pedido de uso emergencial em caráter experimental da vacina Covaxin. A solicitação foi feita pela empresa Precisa Comercialização de Medicamentos.
Após o pedido, agência iniciou a triagem dos documentos já encaminhados. As primeiras 24 horas serão utilizadas para verificação do processo e se os documentos necessários para avaliação estão disponíveis. No caso de falta de informações importantes, a Anvisa poderá solicitar as informações adicionais ao laboratório.
Para sua avaliação, a Anvisa vai utilizar as informações apresentadas junto com o pedido e também as informações encaminhadas anteriormente por meio da submissão contínua.
A análise do pedido de uso emergencial é feita por uma equipe multidisciplinar que envolve especialistas das áreas de registro, monitoramento e inspeção de medicamentos.
Em 4 de junho, a Anvisa autorizou a importação excepcional da Covaxin pelo Ministério da Saúde para distribuição e uso em condições controladas.
O imunizante, no entanto, deverá ser aplicado apenas em adultos, de 18 a 60 anos, e não poderá ser utilizada em gestantes, puérperas, lactantes e indivíduos com comorbidades.
Reportar ErroDeixe seu Comentário
Leia Também

Anvisa proíbe canetas emagrecedoras irregulares no Brasil

Plano de ação em Dourados estabelece medidas para enfrentamento da chikungunya

PM salva bebê em parada cardiorrespiratória em meio ao desespero dos pais em Campo Grande

Capital registra sexto caso de morcego com raiva em 2026

'Avanço', diz Ministério Público sobre o fornecimento de comida nas UPAs e CRSs

Chikungunya avança e faz 7ª vítima em Dourados

Subtenente que atirou na companheira segue vivo em estado grave na Santa Casa

PF intensifica combate a esquema de medicamentos ilegais usados para emagrecimento em MS

Campanha vai aplicar 89 mil doses de vacinas em territórios indígenas