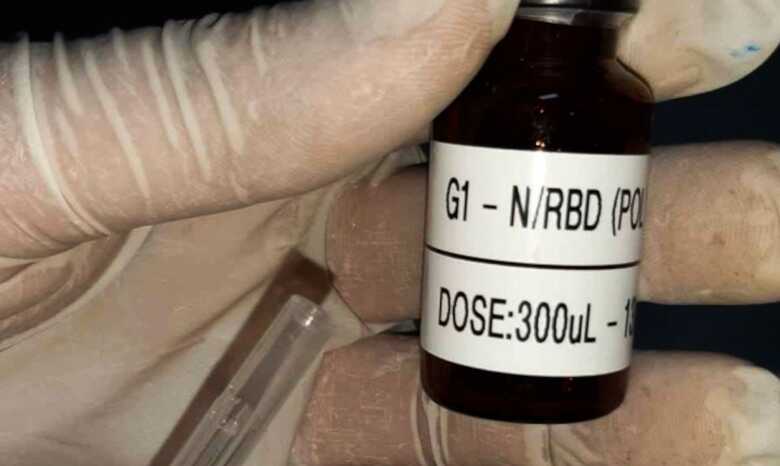
Desenvolvida por pesquisadores da Universidade Federal de Minas Gerais (UFMG) e pela Fundação Oswaldo Cruz (Fiocruz), a vacina SpiN-Tec contra a covid-19, 100% brasileira tem apresentado resultados positivos.
O imunizante não depende de transferência de tecnologia ou de importação. Dados preliminares indicam que ela não apresentou problemas de segurança com os voluntários e tem potencial para gerar uma resposta imunológica ao vírus causador da doença.
Depois de passar pela fase pré-clínica, quando os testes realizados em animais de laboratório não apresentaram efeitos colaterais, a fase clínica 1 começou em novembro do ano passado. Até março deste ano, a vacina foi aplicada em 36 pessoas, com idade entre 18 e 54 anos. Os dados estão em análise pelos pesquisadores e devem ser apresentados ainda neste mês para a Agência Nacional de Vigilância Sanitária (Anvisa).
A expectativa é que a fase clínica 2 comece no início de junho com 372 voluntários entre 18 e 85 anos. Na fase 2, o foco dos testes é na imunogenicidade, ou seja, verificar o nível de anticorpos gerados e a resposta dos linfócitos na proteção do organismo.
Helton Santiago, coordenador dos testes clínicos da vacina e professor do Departamento de Bioquímica e Imunologia do Instituto de Ciências Biológicas (ICB) da UFMG, explica que, ao contrário do que ocorreu nos testes das primeiras vacinas contra a covid-19, desta vez o objetivo é testar a eficácia da SpiN-Tec como dose de reforço.
“Seria muito difícil, neste momento, ir atrás dos poucos no Brasil que não foram vacinados com nenhuma dose. A estratégia do CT Vacinas da UFMG foi mesmo desenvolver um imunizante que sirva como reforço. O nosso tem o diferencial de focar na imunidade celular. Quando os anticorpos neutralizantes falham, é a imunidade celular que segura a infecção e a deixa leve. Então, a gente acredita que essa vacina vai ser ideal para proteger contra novas variantes. Enquanto outras vão perder a eficácia, a nossa não deixa as variantes escaparem da imunidade”.
O cronograma prevê o início da fase 3 em dezembro deste ano ou em janeiro de 2024. Até o início de 2025 a vacina pode estar disponível para a população.
Os testes contam com investimentos da Fundação de Amparo à Pesquisa do Estado de São Paulo (Fapesp), da Rede Vírus do Ministério da Ciência, Tecnologia e Inovações (MCTI), da prefeitura de Belo Horizonte e da Fundação de Amparo à Pesquisa do Estado de Minas Gerais (Fapemig).
Reportar Erro
Deixe seu Comentário
Leia Também

Anvisa manda recolher lotes de fĂłrmula infantil da Danone

Câncer colorretal pode causar 635 mil mortes no Brasil até 2030, diz INCA
MP investiga fila por consultas de hepatologia no SUS em Campo Grande

Hemosul Móvel percorre MS para ampliar doações de sangue e cadastro de medula óssea

Humap realiza procedimento raro com apoio de tecnologia avançada
Saúde está em alerta máximo por aumento do sarampo nas Américas
Vacina da herpes-zóster é segura para pacientes reumáticos, diz estudo

População sofre com longa espera por exame cardĂaco, e investigação Ă© aberta na Capital

Anvisa recolhe esmaltes em gel com substância proibida